La fertilité chimique
Elle se définit par l’aptitude d’un sol à créer et à maintenir un statut chimique caractérisé par son pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
|
L'acidité du sol mesurée par le pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
L'acidification des sols non calcaires est un phénomène naturel. Elle est due à un bilan positif de protons. La production de protons dans le sol est liée pour une large part aux cycles de l'azote, du carbone et du soufre (pour plus de détails, consulter les Cycles Bio-Géo-Chimiques).
Le pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
est variable dans le temps : Il augmente en hiver et diminue en été, où il y a plus de production de protons H+.
Le pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
d'un sol est la mesure de la quantité d'ions H+ libres dans l'eau (pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
eau).
Plus le sol est filtrant ou sableux, plus l’amplitude intra annuelle est importante (jusqu’à 1 point d’écart).
Puisque le pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
eau du sol n’est pas stable dans l’année et sur la profondeur prélevée, il convient de toujours effectuer les mesures dans les mêmes conditions et mêmes période.
pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
= Log (1/H+), simplification de Log (1/Activité de l’ion H3O+ ).
La mesure normalisée du pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
doit se faire sur un rapport volume de terre / volume de solution de 1/5 (NF X 31-117).
Le pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
est une mesure conventionnelle permettant les comparaisons. Le pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
de la solution du sol in situ peut être très différent du pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
mesuré au laboratoire.
Un sol est dit
- acide pour un pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
eau inférieur à 6,8 - neutre pour un pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
eau compris entre 6,8 et 7,2 - alcalin pour un pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
en eau supérieur à 7,2.
Le pouvoir tampon du sol est la faculté de résister aux variations rapides du pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
.
Il est d'autant plus fort qu'il est riche en argile et en humus.
Dans les écosystèmes cultivés, agricoles ou forestiers, l'homme est susceptible d'accélérer ou de ralentir le processus d'acidification par ses pratiques culturales, en particulier avec l'apport raisonné d'amendements basiques.
Le potentiel Redox
L’aération du sol favorise les réactions d’oxydation dans le sol, à l’inverse l’excès d’eau crée des conditions réductrices souvent défavorables à l’activité biologique et à la croissance des racines. Ces conditions modifient aussi la biodisponibilitébiodisponibilitéDéfinition: Caractéristique d’une espèce chimique présente dans le sol lui conférant la possibilité d’être absorbée par une culture....
de certains éléments nutritifs en modifiant leur spéciation (valence des ions métalliques qui peuvent s’insolubiliser).
La biodisponibilitébiodisponibilitéDéfinition: Caractéristique d’une espèce chimique présente dans le sol lui conférant la possibilité d’être absorbée par une culture....
des éléments nutritifs
La quantité tout autant que la biodisponibilitébiodisponibilitéDéfinition: Caractéristique d’une espèce chimique présente dans le sol lui conférant la possibilité d’être absorbée par une culture....
de chaque élément nutritif sont des éléments à prendre en compte. L’analyse chimique tente de reproduire par des extractants l’action des racines. Elle fournit un indicateur indispensable de la biodisponibilitébiodisponibilitéDéfinition: Caractéristique d’une espèce chimique présente dans le sol lui conférant la possibilité d’être absorbée par une culture....
des éléments et permet le suivi à long terme des réserves pour des éléments comme le phosphore, le potassium et le magnésium.
Les cations échangeables
Un sel minéral en solution dans l'eau du sol s'y trouve à l'état dissocié, scindé en deux ions : l'anion, chargé négativement et le cation, chargé positivement.
Le complexe argilo-humique possède la propriété de retenir à sa surface les cations de la solution du sol (on parle aussi du pouvoir adsorbant). L'humus a un pouvoir adsorbant quatre fois plus important que celui des argiles.
Complexe adsorbant
![]()
Les cations sont des éléments minéraux qui s'échangent facilement entre la solution du sol et le complexe ou capacité d'échange cationique (CEC). Ils sont aussi absorbés par les racines qui utilisent cette réserve de cations pour s'alimenter. On considère qu'ils sont bio-disponibles pour la plante.
Cas particulier : Les engrais azotés minéraux apportent l'azote :
- soit sous forme de cation NH4+, qui peut se fixer sur la capacité d'échange cationique,
- soit sous forme de l'anion nitrate NO3- qui n'est pas retenu par le complexe et est mobile dans la solution du sol.
L'importance du complexe adsorbant et son taux de saturation
L’hydrogène est le cation le plus énergiquement retenu par la capacité d’échange cationiquecapacité d’échange cationiqueDéfinition: Mesure chimique conventionnelle réalisée sur un échantillon de terre, destinée à approcher la capacité d’un sol à stocker de façon réversible des éléments minéraux échangeables notamment des cations....
. Si l’acidité du sol est forte les ions H+ déplacent les autres cations et occupent les sites d’adsorption sur la capacité d’échange cationiquecapacité d’échange cationiqueDéfinition: Mesure chimique conventionnelle réalisée sur un échantillon de terre, destinée à approcher la capacité d’un sol à stocker de façon réversible des éléments minéraux échangeables notamment des cations....
.
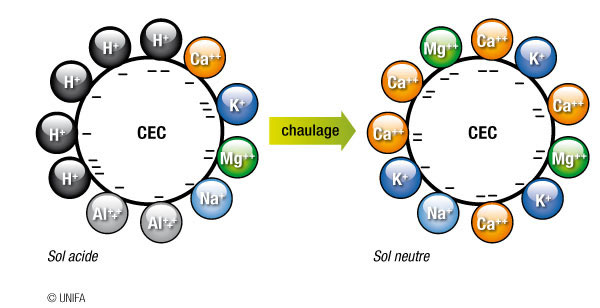
La capacité d'échange d'un sol est saturée quand tous les hydrogènes ou protons H+ sont remplacés par des cations tels que Ca2+, Mg2+ et K+, aussi appelés cations échangeables. Pour neutraliser les ions H+, il faut apporter des radicaux OH- libérés par la chaux ou les carbonates contenus dans les amendements minéraux basiques.
La quantité maximum de cations échangeables qu'un sol peut fixer détermine la Capacité d'échange cationique (C.E.C.). L'augmentation du pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
du sol permet d'augmenter la CEC effective, c'est-à-dire celle qui est disponible pour la mise en réserve des cations échangeables.
Le taux de saturation (S/T) est le rapport entre la somme des cations échangeables extraits par une méthode conventionnelle et la CEC mesurée le plus souvent à un pHpHDéfinition: Notation qui rend compte de la concentration en ions H+ du milieu et désigne ainsi le caractère très acide (pH 4 à 5,5), acide (5,5 à 6,8), neutre (6,8 à 7,2) ou alcalin (supérieur à 7,2) d’un sol....
standard ramené à 7 (CEC Metson). Le taux de saturation est exprimé en % et varie de 50-60% en sols acides à plus de 120% dans les sols calcaires.

